
2020年3月28日,美国FDA发布了个人防护装备紧急使用授权(Emergency Use Authorizations,简称EUA),其中包括《未经NIOSH批准的进口一次性过滤式呼吸防护口罩》,列举了“经过设计、评估和验证后符合以下性能标准的,并具有相应可接受的产品分类的口罩”要求,具体列表如下:
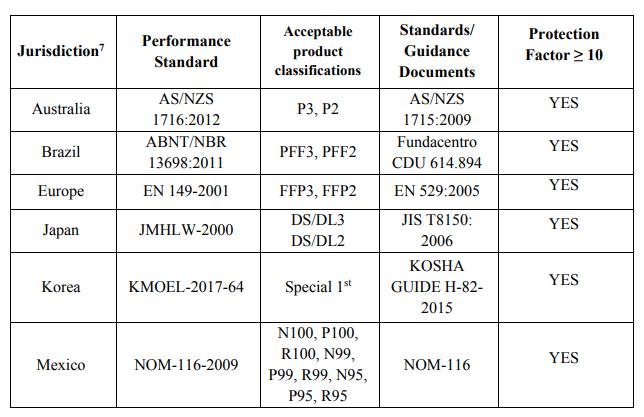
值得注意的是,美国疾病控制与预防中心(CDC)曾经于3月17日发布《优化N95口罩供应策略:危机/替代策略》,其中将根据中国GB2626-2006和GB/T 18664—2002标准生产的口罩列为N95口罩的合适替代品。但是,3月28日美国FDA发布的此份EUA中,中国的GB2626-2006和GB/T18664-2002不再包含在第一类要求内。
全文见:
https://www.fda.gov/media/136403/download
附:此EUA的部分内容原文译文列出如下:
Respirators Eligible for Authorization under this EUA Respirators meeting the criteria in the following two categories are eligible for authorization under this EUA as described in this section (Scope of Authorization (Section II)). Respirators that satisfy the eligibility criteria in numerals 1 and/or 2